Blokada splotu ramiennego – dostęp pomiędzy mięśniami pochyłymi
Blokada splotu ramiennego z dostępu pomiędzy mięśniami pochyłymi jest najbardziej proksymalnym dostępem. Wykonujemy ją na poziomie korzeni splotu ramiennego.
Wskazania:
- Operacje w obrębie barku oraz proksymalnej części ramienia (1/3 bliższa).
Przeciwwskazania:
Bezwzględne:
- Odmowa pacjenta
- Infekcja w miejscu wkłucia
- Uczulenie na środki miejscowo znieczulające
- Ciężkie schorzenia układu oddechowego lub patologiczna otyłość z uwagi na ryzyko porażenia nerwu przeponowego (VC < 1l)
Względne:
- Brak możliwości współpracy z pacjentem
- Koagulopatie
- Deficyty neurologiczne w obrębie obszaru zaopatrywanego przez splot ramienny
- POChP
- Inne schorzenia powodujące obniżenie tolerancji na zmniejszenie VC o ok. 25 % (np. otyłość)
Zalety:
- Struktury nerwowe znajdują się bardzo powierzchownie.
- Szybki początek wystąpienia blokady.
Wady:
- Duże ryzyko uszkodzenia struktur nerwowych (największe spośród wszystkich blokad kończyny górnej).
- Jednostronne porażenie przepony (czytaj niżej) .
- Niepełna blokada w obrębie przyśrodkowej części ramienia oraz przedramienia i ręki.
Ułożenie pacjenta:
- Pacjent w ułożeniu na plecach z lekko uniesioną górną połową ciała. Głowa skierowana w kierunku przeciwnym do wykonywanej blokady. Pod bark po stronie operowanej możemy podłożyć „wałek” co polepsza dostęp do okolicy bocznej szyi.
Lokalizacja i sonoanatomia:
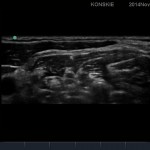
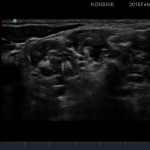
- W celu uwidocznienia splotu w okolicy pomiędzy mięśniami pochyłymi, liniową głowicę USG przykładamy w obrębie trójkąta bocznego szyi, kilka centymetrów powyżej obojczyka, bezpośrednio nad żyłą szyjną zewnętrzną, starając się uwidocznić tętnicę i żyłę szyjną oraz zarys mięśnia mostkowo-obojczykowo-sutkowego. Po uwidocznieniu naczyń szyjnych przesuwamy głowicę w kierunku grzbietowym, gdzie staramy się zlokalizować hipoechogeniczne pnie splotu ramiennego „wciśnięte” pomiędzy mięsień pochyły przedni i środkowy. W celu optymalizacji obrazu przesuwamy głowicę w kierunku góra-dół oraz staramy się odnaleźć odpowiedni kąt skanowania tak aby czoło głowicy znajdowało się prostopadle do struktur nerwowych .
- Inną polecaną metodą jest uwidocznienie splotu ramiennego w okolicy nadobojczykowej a następnie przesuwając głowicę w kierunku dogłowowym „śledzimy” splot (tzw. nerve tracing), odnajdując jego struktury w szczelinie międzypochyłej.
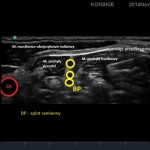
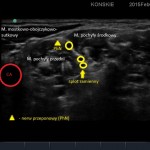
- W obrazie ultrasonograficznym możemy także odnaleźć powierzchownie położoną blaszkę przedkręgową powięzi szyi (hiperechogeniczna linijna struktura), którą przykryty jest splot, zarys mięśnia mostkowo-obojczykowo-sutkowego a także głębsze struktury takie jak tętnica kręgowa i wyrostki poprzeczne kręgów szyjnych. W bezpośrednim sąsiedztwie splotu, na przedniej powierzchni mięśnia pochyłego przedniego, tuż pod blaszką przedkręgową położony jest nerw przeponowy. Takie implikacje anatomiczne sprawiają, iż jednostronna blokada nerwu przeponowego jest praktycznie nieunikniona przy wykonywaniu blokady splotu ramiennego z dostępu pomiędzy mięśniami pochyłymi z wykorzystaniem standardowych dawek LMZ (Film poniżej).
- Dość często przez okolicę trójkąta bocznego szyi przebiega tętnica poprzeczna szyi (gałąź pnia tarczowo-szyjnego) warto zatem przed przystąpieniem do blokady przeskanować okolicę za pomocą opcji color Doppler aby uniknąć nakłucia tej struktury.
Kliknij na galerię aby powiększyć
- Sonoanatomi splotu ramiennego w szczelinie międzypochyłej
- Sonoanatomi splotu ramiennego w szczelinie międzypochyłej
- Nerw przeponowy, splot ramienny
- Nerw przeponowy, splot ramienny
- Anatomia nerwu przeponowego, BP – splot ramienny
Technika wykonania blokady:
- Wykorzystując technikę in plane igłę wprowadzamy najczęściej od strony grzbietowej, idąc przez mięsień pochyły środkowy, w kierunku szczeliny międzypochyłej i splotu ramiennego. Splot otacza blaszka przedkręgową powięzi szyi, którą należy przebić aby uzyskać dostęp do właściwej przestrzeni powięziowej. Staramy się umieścić koniec igły pomiędzy korzeniem C5 a C6. W celu potwierdzenia prawidłowego położenia końcówki igły, po próbie aspiracji, podajemy najpierw 0,5 -1ml LMZ, uważnie obserwując rozprzestrzenianie się leku. Do wykonania skutecznej blokady nie jest konieczne repozycja igły a całą objętość leku możemy zdeponować w pierwotnym położeniu igły (pomiędzy C5 a C6).
Kliknij na galerię aby powiększyć
- Blokada splotu ramiennego z dostępu między mięśniami pochyłymi – technika in plane.
- Blokada splotu ramiennego z dostępu między mięśniami pochyłymi – technika out of plane.
- Technika out of plane może być bardzo przydatna w przypadku wykonywania tej blokady. Jej zaletą jest krótsza droga igły (zwykle splot znajduje się na głębokości ok 1 cm) i co za tym idzie mniejsza traumatyzacja tkanek. Dodatkowo za wyborem tej techniki przemawia mniejsze ryzyko uszkodzenia struktur nerwowych takich jak nerw grzbietowy łopatki, nerw nadłopatkowy, piersiowy długi, które zwykle znajdują się na drodze igły wprowadzanej in plane (w obrębie mięśnia pochyłego środkowego)!!!
Zeskanuj poniższy QR kod aby wyświetlić film
- Android
- iPhone
Ciągłą blokada splotu ramiennego:
- Złoty standard prowadzenia analgezji po zabiegach artroskopowych oraz otwartych stawu barkowego. Inne wskazania to prowadzenie analgezji po dużych zabiegach w obrębie kości ramiennej w części proksymalnej.
- Zaleca się wykonywanie tej blokady z wykorzystaniem techniki out of plane, umieszczając koniec cewnika w bruździe międzypochyłej poniżej powięzi przedkręgowej w bezpośrednim sąsiedztwie splotu (optymalnie na poziomie pomiędzy pniem środkowym i dolnym).
- Położenie końca cewnika możemy zidentyfikować podając niewielką objętość LMZ obserwując jego rozprzestrzenianie się.
Dawka leku miejscowo znieczulającego:
- Blokady „single shot”: 10 do 15ml LMZ (0,25 -0,5% Bupiwakaina bądź 0,5% Ropiwakaina, 1-2% Lignokaina).
- Ciągła blokada: 0,125-0,25% Bupiwakaina, 0,2% Ropiwakaina, przepływ – 4 – 8 ml/h, bolus 3 – 5 ml, lock-out 20 – 60 min (pompa PCA) bądź ciągła podaż LMZ z wykorzystaniem pompy elastomerycznej.
- Dawka u pacjentów pediatrycznych: średnio 0,1 -0,2 ml/kg 0,2% ropiwakainy bądź 0,25% bupiwakainy.
Powikłania:
- Porażenie nerwu przeponowego (nerw przeponowy przebiega w bezpośrednim sąsiedztwie splotu, na przedniej powierzchni mięśnia pochyłego przedniego, porażenie może powodować trudności w oddychaniu szczególnie u osób z chorobami płuc lub znaczną otyłością) – przy użyciu standardowych dawek LMZ (>10 ml) porażenie n. przeponowego towarzyszy praktycznie każdej blokadzie.
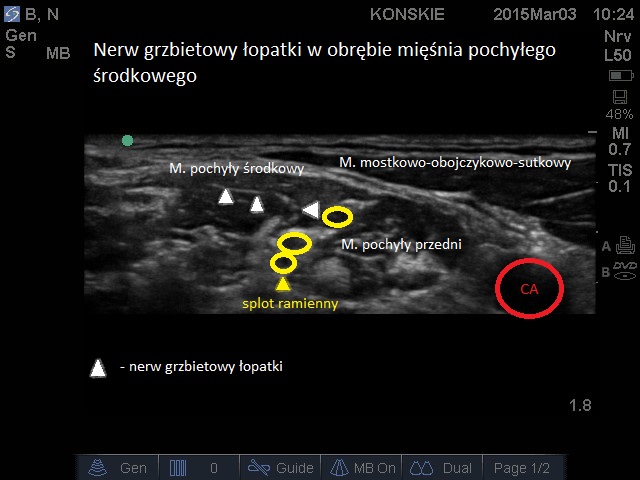
- W trakcie wykonywania blokady metodą in-plane istnieje dość duże ryzyko uszkodzenia nerwu grzbietowego łopatki (który na tym poziomie przebiega w obrębie mięśnia pochyłego środkowego) oraz piersiowego długiego (patrz galeria poniżej).
Kliknij na galerię aby powiększyć
- Nerw grzbietowy łopatki
- Nerw grzbietowy łopatki
- Nakłucie i uszkodzenie struktur nerwowych (największe ryzyko spośród wszystkich wykonywanych blokad!!!).
- Porażenie nerwu krtaniowego wstecznego (chrypka).
- Znieczulenie zewnątrzoponowe w odcinku szyjnym (rzadko spotykane powikłanie przy wykorzystaniu USG).
- Zespół Hornera.
- Powikłania infekcyjne.
- Toksyczna reakcja na środki miejscowo znieczulające.
- Nakłucie struktur naczyniowych z powstaniem krwiaka (duże naczynia szyjne, tętnica poprzeczna szyi, tętnica kręgowa).
- Odma opłucnowa
- Odruch Bezolda-Jarisha (nagła bradykardia z hipotensją, 15-30%)
Uwagi:
- Czuciowe unerwienie okolicy obręczy barkowej (dół nadobojczykowy, okolica obojczyka i górny obszar barku) pochodzi ze splotu szyjnego powierzchownego (głównie nerwy nadobojczykowe). W celu uzyskania pełnej blokady czuciowej u pacjentów poddawanych zabiegom w obrębie stawu barkowego, konieczne jest więc wykonanie dodatkowo blokady splotu szyjnego.
- Blokadę z dostępu między mięśniami pochyłymi najczęściej wykonujemy na poziomie korzeni C5-C7. Blokada zwykle nie obejmuje korzenia C8/Th1 (pień dolny) i co za tym idzie przyśrodkowa część ramienia oraz przedramienia a także fragment dłoni zaopatrywany przez n. łokciowy pozostają nieznieczulone. Dlatego też dostęp ten nie powinien być wykonywany do zabiegów w obrębie przedramienia i ręki a zarezerwowany tylko i wyłącznie do operacji barku oraz 1/3 proksymalnej ramienia.
Diagnostyka porażenia nerwu przeponowego:
- Blokada splotu ramiennego z dostępu pomiędzy mięśniami pochyłymi wiąże się nawet ze 100% ryzykiem wystąpienia jednostronnego porażenia nerwu przeponowego (HDP – hemidiaphragmatic paresis), co może skutkować 25 – 30% redukcją czynnościowej pojemności zalegającej (szczególnie groźne u pacjentów z chorobami układu oddechowego oraz patologiczną otyłością).
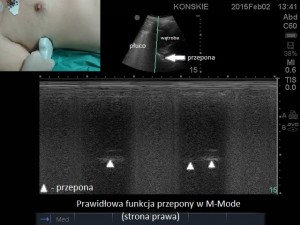
- W celu diagnostyki porażenia przepony możemy użyć USG wykorzystując tryb obrazowania ruchu – M-Mode:
- Głowicę USG typu covex przykładamy w płaszczyźnie poprzecznej w linii pachowej środkowej po stronie wykonanej blokady, tak aby uwidocznić przeponę.
- Uruchamiamy tryb M-Mode tak aby linia skanowania przechodziła przez przeponę (poniżej zdjęcia prawidłowej funkcji przepony oraz jej porażenia):
Kliknij na galerię aby powiększyć
- Prawidłowa funkcja przepony w M-Mode
- Porażenie przepony (strona lewa) w M-Mode
- Aby zminimalizować ryzyko HDP zalecane jest wykonywanie tzw. „low volume block” z wykorzystanie niskich objętości – 5 ml LMZ. Postępowanie taki zmniejsza częstość występowania HDP nawet o połowę (porównując z dawką 10 oraz 20 ml), nie powodując przy tym obniżenia jakości blokady oraz zwiększenia zapotrzebowania na opioidy po zabiegu.
- Wykonanie blokady bardziej dystalnie (na poziomie wyrostka poprzecznego kręgu C7) może także zmniejszyć ryzyko HDP, gdyż na tej tej wysokości dystans pomiędzy nerwem przeponowym a splotem ramiennym ulega zwiększeniu.
- Zdjęcie RTG klatki piersiowej może także być wykorzystywane w celu diagnostyki jednostronnego porażenia przepony (wysoko uniesiona kopuła przepony), jest to jednak dużo mniej czułe badanie w porównaniu do USG.
Przydatne artykuły:
- Borgeat A. and Ekatodramis G. (2002). Anaesthesia for shoulder surgery. Best Practice and Research Clinical Anaesthiology, 16, 211-25.
- Brull R., McCartney C.J., Chan V.W. and El-Beheiry H. (2007). Neurological complications after regional anesthesia: contemporary estimates of risk. Anesthesia and Analgesia, 104, 965-74.
- Chelly J.E., Greger J., Al Samsam T et al. (2001). Reduction of operating and recovery room times and overnight hospital stays with interscalene blocks as sole anesthetic technique for rotator cuff surgery. Minerva Anestesiologica, 67, 613-19.
- Cummings K.C. 3rd, Napierkowski D.E., Parra-Sanchez I. et al. (2011). Effect of dexamethasone on the duration of interscalene nerve blocks with ropivacaine or bupivacaine. British Journal of Anaesthesia, 107, 446-53.
- Desmet M., Braemsm Reynovet et al. (2013). IV and perineural dsexamethasone are equivalent in increasing the analgesic duration of a single shot interscalene block with ropivicaine for shoulder surgery: a prospective randomised placebo controlled study. Br J Anaes, 111: 445-52.
- Fredrickson M.J., Abeysekera A. and White R. (2012). Randomized study of the effect of local anesthetic volume and concentration on the duration of peripheral nerve blockade. Regional Anesthesia and Pain Medicine 37, 495-501.
- Fredrickson M.J., Ball C.M. and Dalgleish A.J. (2010). Analgesic effectiveness of a continuous versus single-injection interscalene block for minor arthroscopic shoulder surgery. Regional Anesthesia and Pain Medicine, 35, 28-33.
- Gadsden J., Gratenstein K. and Hadzic A. (2010). Intraneural injection and peripheral nerve injury. International Anesthesiology Clinics, 48, 107-15.
- Gadsden J., Hadzic A., Gandhi K. et al. (2011). The effect of mixing 1.5% mepivacaine and 0.5% bupivacaine on duration of analgesia and latency of block onset in ultrasound-guided interscalene block. Anaesthesia and Analgesia, 112, 47176.
- Gelfand H.J., Ouanes J.P., Lesley M.R. et al. (2011). Analgesic efficacy of ultrasound-guided regional anesthesia: a meta-analysis. Journal of Clinical Anesthesia 23, 90-96.
- Ilfeld B.M., Morey T.E., Wright T.W., Chidgey L.K. and Enneking F.K. (2003). Continuous interscalene brachial plexus block for postoperative pain control at home: a randomized, double-blinded, placebo-controlled study. Anesthesia and Analgesia, 96,1089-95.
- Kapral S., Greher M,. Huber G. et al (2008). Ultrasonography guidance improves the success rate of interscalene brachial plexus blockade. Regional Anesthesia and Pain Medicine, 33, 253-58.
- Knoblanche G.E. (1979). The incidence and aetiology of phrenic nerve blockade associated with supraclavicular brachial plexus block. Anaesthesia and Intensive Care, 7, 346-49. ne, 31, 192-95.
- Krone S.C., Chan V.W., Regan J. et al. (2001). Analgesic effects of low-dose ropivacaine for interscalene brachial plexus block for outpatient shoulder surgery-a dose-finding study. Regional Anesthesia and Pain Medicine 26, 439-43.
- Liu S.S., Gordon M.A., Shaw P.M., Wilfred S., Shetty T. and Yadeau J.T. (2010) A prospective clinical registry of ultrasound-guided regional anesthesia for ambulatory shoulder surgery. Anesthesia and Analgesia, 111, 617-23.
- Macfarlane A.J., Bhatia A. and Brull R. (2011). Needle to nerve proximity: what do the animal studies tell us? Regional Anesthesia and Pain Medicine, 36, 290-302.
- Maybin J., Townsley P., Bedforth N. and Allan A. (2011). Ultrasound guided supraclavicular nerve blockade: first technical description and the relevance for shoulder surgery under regional anaesthesia. Anaesthesia, 66, 1053-55.
- McNaught A., Shastri U., Carmichael N. et al. (2011). Ultrasound reduces the minimum effective local anaesthetic volume compared with peripheral nerve stimulation for interscalene block. British Journal of Anaesthesia 106, 124-30.
- Neal J.M., Gerancher J.C., Hebl J.R. et al. (2008). Upper extremity regional anesthesia: essentials of our current understanding, 2008. Regional Anesthesia and Pain Medicine, 34, 134-70.
- Pöpping D.M., Elia N., Marret E., Wenk . and Tramèr M.R. (2009). Clonidine as an adjuvant to local anesthetics for peripheral nerve and plexus blocks: a meta-analysis of randomized trials. Anesthesiology, 111, 406-15.
- Renes S.H., Rettig H.C., Gielen M.J., Wilder-Smith O.H. and van Geffen G.J. (2009). Ultrasound-guided low-dose interscalene brachial plexus block reduces the incidence of hemidiaphragmatic paresis. Regional Anesthesia and Pain Medicine, 34, 498-502.
- Renes S.H., Spoormans H.H., Gielen M.J., Rettig H.C. and van Geffen G.J. (2009). Hemidiaphragmatic paresis can be avoided in ultrasound-guided supraclavicular brachial plexus block. Regional Anesthesia and Pain Medicine, 34, 595-99.
- Riazi S., Carmichael N., Awad I., Holtby R.M. and McCartney C.J. (2008). Effect of local anaesthetic volume (20 vs 5 ml) on the efficacy and respiratory consequences of ultrasound-guided interscalene brachial plexus block. British Journal of Anaesthesia,101, 549-56.
- Sinha S.K., Abrams J.H. and Weller R.S. (2007). Ultrasound-guided interscalene needle placement produces successful anesthesia regardless of motor stimulation above or below 0.5 mA. Anesthesia and Analgesia, 105, 848-52.
- Sites B.D., Macfarlane A.J., Sites V.R. et al. (2010). Clinical sonopathology for the regional anesthesiologist: part 1: vascular and neural. Regional Anesthesia and Pain Medicine, 35, 272-80.
- Sites B.D., Macfarlane A.J., Sites V.R. et al.(2010). Clinical sonopathology for the regional anesthesiologist: part 2: bone, viscera, subcutaneous tissue, and foreign bodies. Regional Anesthesia and Pain Medicine, 35, 281-89.
- Spence B.C., Beach M.L., Gallagher J.D. and Sites B.D. (2011) Ultrasound-guided interscalene blocks: understanding where to inject the local anaesthetic. Anaesthesia, 66, 509-14.
- Verelst P. and van Zundert A. (2013). Respiratory impact of analgesic strategies for shoulder surgery. Regional Anesthesia and Pain Medicine, 38, 50-53.
- Vieira P.A., Pulai I., Tsao G.C., Manikantan P., Keller B. and Connelly N.R. (2010). Dexamethasone with bupivacaine increases duration of analgesia in ultrasoundguided interscalene brachial plexus blockade. European Journal of Anaesthesiology, 27, 285-88.