Ogólnoustrojowa toksyczność środków miejscowo znieczulających (LAST)
Środki miejscowo znieczulające – to grupa związków powodujących odwracalną blokadę przewodzenia bodźców nerwowych w określonej okolicy ciała (dystalnie od miejsca wstrzyknięcia). Są słabo zasadowymi aminami aromatycznymi, słabo rozpuszczalnymi w wodzie, składającymi się z części hydrofilnej i lipofilnej, które są połączone łańcuchem węglowodorowym. W zależności od typu wiązania obu części (ester lub amid) możemy je podzielić na aminoestry (kokaina, benzokaina, prokaina, ametokaina, chloroprokaina, tetrakaina) i aminoamidy (prilokaina, lidokaina, mepiwakaina, bupiwakaina, lewobupiwakaina, ropiwakaina, etidokaina).
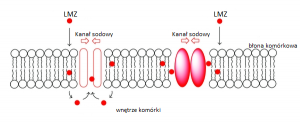
Mechanizm działania opiera się na bezpośredniej blokadzie swoistych jonowo kanałów sodowych w błonie nerwów co skutkuje zmniejszeniem amplitudy i szybkości wzrostu potencjału czynnościowego oraz zwiększeniem progu pobudliwości i okresu refrakcji, aż do całkowitego zniesienia ich pobudliwości. Siła, szybkość rozpoczęcia, czas działania a także właściwości toksyczne zależą głównie od cech fizykochemicznych substancji, jak również dawki, miejsca wstrzyknięcia, alkalizacji roztworu czy też dodatku środków obkurczających naczynia. Biorąc pod uwagę siłę działania możemy wyróżnić środki o słabej (prokaina), średniej (lidokaina, mepiwakaina, prilokaina, chloroprokaina) i dużej sile działania (bupiwakaina, lewobupiwakaina, ropiwakaina, etidokaina, tetrakaina). Innym klinicznie ważnym podziałem jest klasyfikacja według czasu działania znieczulenia: krótki (prokaina, chlorprokaina), średni (lidokaina, mepiwakaina, prilokaina) i długi czas działania (ropiwakaina, bupiwakaina, lewobupiwakaina, etidokaina, tetrakaina). W praktyce klinicznej najczęściej stosuje się lidokainę, bupiwakainę, lewobupiwakainę oraz ropiwakainę.
- Mechanizm działania LMZ
- Mechanizm działania LMZ
LAST
Środki miejscowo znieczulające mogą wywoływać różne objawy niepożądane, spośród których ogólnoustrojowe działania toksyczne (LAST – Local Anesthetic Systemic Toxicity) odgrywają najważniejszą rolę. Zwykle spowodowane są przedawkowaniem lub przypadkowym wstrzyknięciem donaczyniowym, dlatego należy zawsze monitorować podstawowe parametry życiowe, zachować szczególną ostrożność i uwzględnić czynniki tj. miejsce i sposób iniekcji, rodzaj i dawkę leku miejscowo znieczulającego, dodatek środka obkurczającego naczynia oraz indywidualną zmienność pacjentów (ogólny stan, dystrybucja w organizmie i metabolizm ). Objawiają się głównie jako zaburzenia ośrodkowego układu nerwowego i układu sercowo-naczyniowego.
Neurotoksyczność
Do typowych objawów wystąpienia neurotoksyczności spowodowanej przez środki miejscowo znieczulające (poza tachykardią) zaliczamy:
- parestezje ust, języka oraz dłoni
- metaliczny smak, senność,
- zawroty głowy,
- dzwonienie w uszach,
- niewyraźna mowa,
- drżenia mięśniowe,
- oczopląs,
- zaburzenia widzenia.
- Drgawki uogólnione,
- Śpiączka
Są to tzw. objawy ostrzegawcze, które mogą wystąpić po znacznie mniejszych dawkach LMZ w porównaniu do dawek kardiotoksycznych. Istotnie kliniczne jest jak najszybsze rozpoznanie działania toksycznego i odpowiednio szybka reakcja.
Przy wystąpieniu objawów ostrzegawczych należy:
- natychmiast przerwać iniekcję leku,
- podać 100% tlen,
- nie dopuszczać do rozwoju hipoksji oraz kwasicy, które nasilają toksyczność środków miejscowo znieczulających (powstaje „pułapka jonowa”),
- w razie wystąpienia drgawek lekiem z wyboru według najnowszych doniesień powinny być benzodwuazepiny,
- przy przedłużających się drgawkach, aby zapobiec rozwojowi hipoksji oraz kwasicy, należy rozważyć podanie środków zwiotczających mięśnie, intubację oraz wentylację mechaniczną.
Kardiotoksyczność
Środki miejscowo znieczulające, w przypadku ich przedawkowania, wpływają na układ sercowo-naczyniowy poprzez zmniejszenie kurczliwości mięśnia sercowego, zaburzenia automatyki i spadek szybkości przewodzenia pobudzeń oraz rozszerzenie naczyń. Po wstępnej fazie stymulacji wskutek pobudzenia OUN – tachykardia i hipertonia, następuje faza depresji – pogłębiające się zmniejszenie kurczliwości i pojemności minutowej serca, spadek ciśnienia tętniczego, ciężkie zaburzenia rytmu pod postacią ekstrasystolii komorowych, aż do zatrzymania akcji serca. Warto podkreślić, iż siła działania środka miejscowo znieczulającego koreluje z działaniem toksycznym zarówno na układ krążenia, jak i OUN ale nie zawsze kardiotoksyczny wpływ jest poprzedzony reakcją z OUN– bupiwakaina może wywołać komorowe zaburzenia rytmu serca bez wywoływania uogólnionych drgawek. W razie wystąpienia objawów toksyczności należy jak najszybciej wdrożyć standardowe postępowanie zapobiegające zaburzeniom krążenia i hipotensji – udrożnienie dróg oddechowych, podaż 100% tlenu, płynów, leków krążeniowych oraz rozważyć podanie 20% roztworu lipidowego w postaci bolusa w dawce 1,5 ml/kg. Gdy dojdzie do zatrzymania akcji serca należy postępować zgodnie z wytycznymi RKO, z uwzględnieniem następujących modyfikacji:
- Redukcja pojedynczych dawek adrenaliny do < 1 mcg/kg,
- Unikanie leków wazopresyjnych, B-blokerów, blokerów kanałów wapniowch i lidokainy (w arytmiach komorowych preferowany amiodaron).
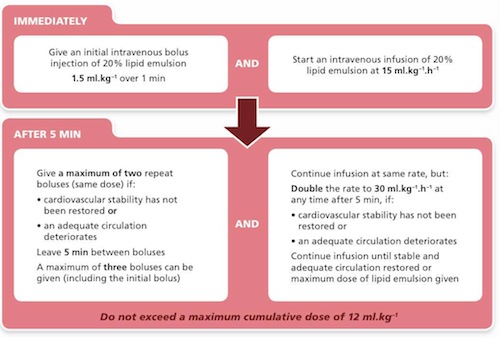
- Natychmiast włączyć dożylną podaż 20% roztworu lipidowego (np. Intralipid) zgodnie ze schematem: 1,5 ml/kg w bolusie w ciągu 1 min, następnie wlew ciągły 15 ml/kg/h, kontynuując RKO. Jeśli nie uzyskano stabilizacji układu krążenia- zwiększyć wlew do 30 ml/kg/h i rozważyć powtórzenie bolusa (max. 3 krotnie w odstępach nie krótszych niż 5 min). Wlew należy kontynuować do monentu przywrócenia stabilności hemodynamicznej lub osiągnięcia maksymalnej rekomendowanej dawki, która wynosi 12 ml/kg.
- Propofol nie powinien być traktowany jako substytut dla emulsji tłuszczowych.
- Powrót spontanicznego krążenia po NZK związanym z LAST może wystąpić nawet po godzinnej resuscytacji.
Należy rozważyć podanie emulsji tłuszczowych przy pojawieniu się pierwszych objawów LAST nie czekając na wystąpienie NZK!!!.
W celu zmniejszenia ryzyka wystąpienia LAST należy kierować się poniższymi wskazówkami:
- Należy zachować szczególną ostrożność i zawsze być przygotowanym na ewentualność wystąpienia LAST (wcześniej opracowany plan postępowania przy wystąpieniu LAST dostępny na każdej sali gdzie wykonywane są procedury z wykorzystaniem LMZ, dokładnie oznakować miejsce przechowywania emulsji tłuszczowych).
- Stały nadzór nad pacjentem oraz ciągłe monitorowanie z wykorzystaniem EKG, pulsoksymetrii, pomiaru BP w trakcie procedury oraz po wykonanej blokadzie (pierwsze objawy LAST mogą się pojawić nawet 30 min po podaniu LMZ).
- Jeśli to możliwe utrzymywać kontakt z pacjentem w trakcie całej procedury, wypytując o ewentualne objawy mogące świadczyć o wystąpieniu LAST.
- Stosujemy tylko lekką sedację (jeśli konieczna), tak aby unikać hipowentylacji co mogłoby skutkować hipoksją, hiperkarbią oraz nasileniem kwasicy.
- Nie przekraczać rekomendowanych maksymalnych dawek środków miejscowo znieczulających.
- Rozważyć zmniejszenie dawki środka miejscowo znieczulającego u pacjentów w podeszłym wieku, obciążonych chorobami układu sercowo-naczyniowego (niska EF) oraz z niskimi wartościami albumin.
- Wykonywanie blokady pod kontrolą wzroku z wykorzystaniem USG pozwala na zmniejszenie dawki LMZ oraz może ograniczyć ryzyko wystąpienia LAST.
- W trakcie podawania LMZ należy utrzymywać stały nacisk głowicy na powierzchnię skóry co ogranicza ryzyko niezamierzonego donaczyniowego podania leku.
- Środek miejscowo znieczulający należy podawać powoli i zawsze pamiętać o próbie aspiracji przed pierwszą dawką oraz po podaniu każdych 4-5 ml LMZ.
- Rozważyć użycie adrenaliny w dawce 5 mcg/ml jako markera donaczyniowego podania LMZ, szczególnie przy wykonywaniu blokad objętościowych (TAP block, fascia iliaca compartment block).
- Należy pamiętać, iż pierwszym objawem wystąpienia LAST najczęściej jest tachykardia, przy jej pojawieniu się konieczne jest przerwanie podawania LMZ.
LMZ w anestezji pediatrycznej
- Noworodki mają obnizony poziom (ok. 40% wartości osób dorosłych) osoczowej kwaśnej α-1 glikoproteiny (białka preferencyjnie wiążącego LMZ). Prawidłowe stężenie osiągane jest zwykle po pierwszym roku życia.
- Obniżony poziom tego białka wiąże się z wysokim stężeniem frakcji wolnej LMZ w osoczu, która to głównie odpowiedzialna jest za działanie toksyczne.
- Niemowlęta do 6 miesiąca życia mają także zwykle obniżony klirens, metabolizm wątrobowy (o ok. 50%) oraz wydłużony czas połowiczej eliminacji LMZ w porównaniu do dorosłych.
- Większa objętość dystrybucji u dzieci może przyczyniać się do kumulacji anestetyku lakalnego w przypadku drugiej i kolejnych iniekcji.
- Dzieci a w szczególności noworodki charakteryzują się dużo większym rzutem serca niż dorosli co powoduje nasiloną absorbcję systemową anestetyków.
- Wszystkie te czynniki zwiększają ryzyko wystąpienia toksyczności LMZ w populacji noworodków i niemowląt. Zatem maksymalna dawka rekomendowana dla amidowych anestetyków lokalnych powinna być zmniejszona o ok. 50% w przypadku tych dwóch grup pacjentów pediatrycznych!
- Obecność hemoglobiny płodowej u niemowląt zwiększa ryzyko wystąpienia methemoglobinemii w przypadku wykorzystania prilokainy.
Przydatne piśmiennictwo:
- Knudsen K, Beckman Suurkula M, Blomberg S, Sjovall J, Edvardsson N. Central nervous and cardiovascular effects of i.v. infusions of ropivacaine, bupivacaine and placebo in volunteers. Br J Anaesth 1997;78:507-14.
- Scott DB, Lee A, Fagan D, Bowler GM, Bloomfield P, Lundh R. Acute toxicity of ropivacaine compared with that of bupivacaine. Anesth Analg 1989;69:563-9.
- Klein SM, Benveniste H. Anxiety, vocalization, and agitation following peripheral nerve block with ropivacaine. Reg Anesth Pain Med 1999;24:175-8.
- Muller M, Litz RJ, Huler M, Albrecht DM. Grand mal convulsion and plasma concentrations after intravascular injection of ropivacaine for axillary brachial plexus blockade. Br J Anaesth 2001;87:784-7.
- Ohmori H, Sato Y, Namiki A. The anticonvulsant action of propofol on epileptiform activity in rat hippocampal slices. Anesth Analg 2004;99:1095-101, table of contents.
- Heavner JE, Arthur J, Zou J, McDaniel K, Tyman-Szram B, Rosenberg PH. Comparison of propofol with thiopentone for treatment of bupivacaine-induced seizures in rats. Br J Anaesth 1993;71:715-9.
- Bai D, Pennefather PS, MacDonald JF, Orser BA. The general anesthetic propofol slows deactivation and desensitization of GABA(A) receptors. J Neurosci 1999;19:10635-46.
- Hara M, Kai Y, Ikemoto Y. Enhancement by propofol of the gamma-aminobutyric acidA response in dissociated hippocampal pyramidal neurons of the rat. Anesthesiology 1994;81:988-94.
- Albright GA. Cardiac arrest following regional anesthesia with etidocaine or bupivacaine. Anesthesiology 1979;51:285-7.
- Reiz S, Nath S. Cardiotoxicity of local anaesthetic agents. Br J Anaesth 1986;58:736-46.
- Sztark F, Malgat M, Dabadie P, Mazat JP. Comparison of the effects of bupivacaine and ropivacaine on heart cell mitochondrial bioenergetics. Anesthesiology 1998;88:1340-9.
- Graf BM, Eberl MD, Abraham BS, Martin MD. Comparison of the direct cardiotoxicity of the isomers of ropivacaine and bupivacaine. Anesthesiology 1998;A876.
- Catterall WA. From ionic currents to molecular mechanisms: the structure and function of voltage-gated sodium channels. Neuron 2000;26:13-25.
- Ohmura S, Kawada M, Ohta T, Yamamoto K, Kobayashi T. Systemic toxicity and resuscitation in bupivacaine-, levobupivacaine-, or ropivacaine-infused rats. Anesth Analg 2001;93:743-8.
- Feldmann HS, Arthur GR, Pitkanen M, Hurley R, Doucette AM, Covino BG. Treatment of acute systemic toxicity after the rapid intravenous injection of ropivacaine and bupivacaine in the conscious dog. Anesth Analg 1991;3:373-84.
- Groban L, Deal DD, Vernon JC, James RL, Butterworth J. Cardiac resuscitation after incremental overdosage with lidocaine, bupivacaine, levobupivacaine, and ropivacaine in anesthetized dogs. Anesth Analg 2001;92:37-43.
- Heavner JE, Pitkanen MT, Shi B, Rosenberg PH. Resuscitation from bupivacaineinduced asystole in rats: comparison of different cardioactive drugs. Anesth Analg 1995;80:1134-9.
- Bruelle P, LeFrant JY, de La Coussaye JE, Peray PA, Desch G, Sassine A, Eledjam JJ. Comparative electrophysiologic and hemodynamic effects of several amide local anesthetic drugs in anesthetized dogs. Anesth Analg 1996;82:648-56.
- Lindgren L, Randell T, Suzuki N, Kytta J, Yli-Hankala A, Rosenberg PH. The effect of amrinone on recovery from severe bupivacaine intoxication in pigs. Anesthesiology 1992;77:309-15.
- Weinberg GL. Current concepts in resuscitation of patients with local anesthetic cardiac toxicity. Reg Anesth Pain Med 2002;27:568-75.
Autorzy: A. Cugowski, W. Gola