Podstawy elektrostymulacji w blokadach nerwów obwodowych
 W celu lokalizacji nerwów obwodowych i splotów oraz depozycji środka miejscowo znieczulającego w bezpośrednim sąsiedztwie nerwu lub kompartmencie zawierającym interesujące nas struktury nerwowe, na przestrzeni lat wykorzystywano różne techniki. Do najstarszej metody wykonywania blokad nerwów obwodowych należy technika oparta o punkty anatomiczne oraz parestezje. Wiąże się ona jednak z dość dużym ryzykiem powikłań neurologicznych związanych z mechanicznym uszkodzeniem struktur nerwowych oraz dużym odsetkiem niepowodzeń. Rozwój techniki dał możliwość dokładniejszej lokalizacji struktur nerwowych poprzez wykorzystanie stymulatorów nerwów a także w ostatnich latach ultrasonografii. Wprowadzenie USG zrewolucjonizowało świat anestezji regionalnej, nie mniej jednak nie spowodowało rezygnacji z wykorzystania neurostymulatora. Co więcej łączenie ze sobą techniki lokalizacji struktur nerwowych opartej o ultrasonografię oraz z użyciem stymulatora nerwów obwodowych (tzw. „dual guidence technique”), może przyczynić się do zwiększenia zarówno skuteczności jak i bezpieczeństwa wykonywanej blokady.
W celu lokalizacji nerwów obwodowych i splotów oraz depozycji środka miejscowo znieczulającego w bezpośrednim sąsiedztwie nerwu lub kompartmencie zawierającym interesujące nas struktury nerwowe, na przestrzeni lat wykorzystywano różne techniki. Do najstarszej metody wykonywania blokad nerwów obwodowych należy technika oparta o punkty anatomiczne oraz parestezje. Wiąże się ona jednak z dość dużym ryzykiem powikłań neurologicznych związanych z mechanicznym uszkodzeniem struktur nerwowych oraz dużym odsetkiem niepowodzeń. Rozwój techniki dał możliwość dokładniejszej lokalizacji struktur nerwowych poprzez wykorzystanie stymulatorów nerwów a także w ostatnich latach ultrasonografii. Wprowadzenie USG zrewolucjonizowało świat anestezji regionalnej, nie mniej jednak nie spowodowało rezygnacji z wykorzystania neurostymulatora. Co więcej łączenie ze sobą techniki lokalizacji struktur nerwowych opartej o ultrasonografię oraz z użyciem stymulatora nerwów obwodowych (tzw. „dual guidence technique”), może przyczynić się do zwiększenia zarówno skuteczności jak i bezpieczeństwa wykonywanej blokady.
Podstawy fizyczne
Neurony, podobnie jak pozostałe komórki ludzkiego organizmu charakteryzują się obecnością przezbłonowego potencjału (różnicą potencjałów pomiędzy wnętrzem a powierzchnią błony komórkowej). Dla niepobudzonych komórek nerwowych oraz mięśniowych potencjał ten zwany też potencjałem spoczynkowym jest ujemny i waha się pomiędzy -65 a -90 mV. Powstanie potencjału spoczynkowego jest spowodowane przede wszystkim ruchem jonów potasu zgodnie z gradientem stężenia z wnętrza na zewnątrz błony komórkowej. Powoduje to pozostanie niewielkiego nadmiaru ładunków ujemnych po wewnętrznej stronie błony. Kiedy na komórkę nerwową zadziała bodziec dochodzi do gwałtownego napływu jonów sodowych do cytozolu co skutkuję zmianą potencjału przezbłonowego oraz depolaryzacją komórki. Jeśli bodziec jest wystarczająco silny i spowoduję, że potencjał komórki przekroczy wartość progową, dojdzie do propagacji fali depolaryzacji wzdłuż włókien nerwowych. Bodziec działający na komórkę nerwową, w celu wywołania skutecznej depolaryzacji, prócz odpowiedniej siły (napięcia) musi charakteryzować się także odpowiednim czasem trwania. Nawet bodziec o wartości progowej działający zbyt krótko na komórkę nie spowoduje powstania potencjału czynnościowego. Krzywą opisującą zależność między napięciem przyłożonym do włókna nerwowego (oś Y), a czasem potrzebnym do zainicjowania potencjału czynnościowego (oś X) nazywamy krzywą pobudliwości włókien nerwowych. Przykładając coraz większe napięcie, czas, w którym obserwuje się początek reakcji (reakcja w postaci potencjału czynnościowego) jest krótszy. Krzywa pobudliwości ma przebieg podobny do wykresu funkcji y=1/x czyli przybiera kształt hiperboli.
- Krzywa pobudliwości dla nerwu ruchowego
- Krzywa pobudliwości dla nerwu czuciowego
Z krzywą łączą się trzy ważne pojęcia:
- Czas użyteczny
- Reobaza
- Chronaksja
Czas użyteczny to najkrótszy czas potrzebny do pobudzenia włókna nerwowego za pomocą maksymalnego bodźca.
Reobaza to najniższe natężenie prądu, którym zostaje wywołany potencjał czynnościowy.
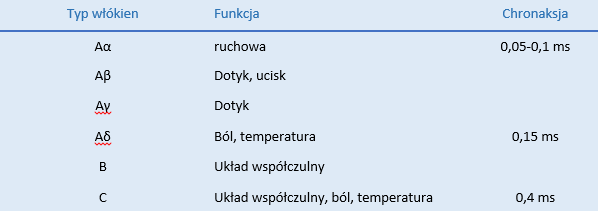
Chronaksja to czas, w którym nastąpi pobudzenie włókna, jeżeli przyłożone zostanie natężenie dwukrotnie większe od reobazy. Chronaksja służy do określania stopnia pobudliwości włókien nerwowych (w zależności od rodzaju włókna waha się w przedziale 0,1-0,5ms). Czas chronaksji jest różny dla różnych rodzajów włókien nerwowych i zależy od ich pobudliwości oraz okresów refrakcji. „Szybkie” włókna nerwowe takie jak włókna motoryczne Aα charakteryzują się krótszym czasem chronaksji w porównaniu do „wolno” przewodzących włókien czuciowych typu Aδ bądź bezmielinowych włókien typu C. Ogólnie rzecz biorąc włókna ruchowe mają krótszy czas chronaksji w porównaniu do włókien czuciowych. Wynika z tego fakt, iż nie można wystymulować włókien czuciowych używając prądu o czasie chronaksji odpowiednim do stymulacji włókien ruchowych. W przełożeniu na praktykę znaczy to, iż w wywołując odpowiedź ruchową (stymulując włókna ruchowe) pacjent nie odczuwa bólu.
Natężenie prądu pomiędzy 0,2 – 0,5 mA, które daje odpowiedź ruchową, uważane jest za wartość odpowiednią do wykonania skutecznej blokady. Należy jednak pamiętać, iż wartość prądu stymulacji nie jest bezpośrednim indykatorem wskazującym na odległość igła-nerw. Można łatwo to zaobserwować wykorzystując USG: lokalizując igłę pod kontrolą wzroku w bezpośrednim sąsiedztwie nerwu, niejednokrotnie w celu jego wystymulowania, konieczne jest użycie dużo wyższych wartości prądu, nawet powyżej 1 mA. Wartość prądu stymulacji < 0,2 mA może świadczyć o śródnerwowym położeniu końcówki igły i najczęściej jest związane z dużym oporem oraz bólem podczas iniekcji LMZ.
Stymulatory nerwów
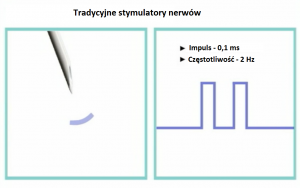
Obecnie dostępne na rynku stymulatory nerwów są generatorami prądu stałego, znaczy to, iż prąd przepływający pomiędzy anodą a katodą jest stały, niezależnie od impedancji tkanek. W obwodzie elektrycznym katodę (biegun ujemny) stanowi igła, anodę (biegun dodatni) – elektroda przyklejona na ciele pacjenta. Najczęściej dostępne na rynku stymulatory generują prąd o natężeniu do 5 mA, krótkim czasie trwania impulsu (od 0,05 -1 ms) oraz częstotliwości 1 -2 Hz. W celu zapewnienia komfortu pacjentowi należy używać jak najniższych początkowych wartości natężenia prądu stymulacji: nie więcej niż 1 mA dla blokad powierzchownych oraz 2 mA (blokady głębokie) oraz jak najniższego czasu trwania impulsu ( optymalnie 0,1 ms – dla nerwów mieszanych, 0,3 dla nerwów czuciowych). Natomiast najbardziej optymalna częstotliwość to 2 Hz. Niekiedy konieczne jest użycie wyższych wartości prądu stymulacji 1,5 – 3 mA (dla głębokich blokad takich jak psoas compartment block), nie należy jednak przekraczać wartości 5 mA. Przy użyciu natężeń > 1,5 mA często obserwujemy bezpośrednią stymulację mięśni, przez które przechodzi igła, takie natężenia powodować mogą także dyskomfort u pacjenta.
Stymulatory z opcją SENSe (Sequential Electrical Nerve Stimulation)
Standardowe stymulatory generują prąd stymulacji o stałym czasie trwania impulsu (najczęściej 0,1 ms) oraz stałej częstotliwości (1 lub 2 Hz). Często jednak spotykamy się z problemem, że wygenerowana odpowiedź ruchowa zanika podczas niewielkich ruchów igłą wykonywanych w celu optymalizacji jej położenia. Technologia SENSe polega na generowaniu dodatkowego dłuższego impulsu (1,0 ms) poprzedzonego dwoma standardowymi impulsami (0,1 ms ). W tym przypadku częstotliwość generowanych impulsów wynosi 3 Hz. Obecność dodatkowego dłuższego impulsu daje możliwość wygenerowania odpowiedzi ruchowej dużo wcześniej niż przy użyciu standardowych stymulatorów oraz optymalizacji położenia igły bez utraty odpowiedzi ruchowej. Dodatkową zaletą jest określenie odległości igła – nerw na podstawie ilości wygenerowanych odpowiedzi ruchowych (1 pobudzenie – zbyt duża odległość igła-nerw, 3 pobudzenia – igłą w bezpośredniej okolicy nerwu).
- Standardowy stymulator
- Technologia SENSe
Przezskórna lokalizacja nerwów
Na rynku dostępne są także stymulatory dające możliwość przezskórnego mapowania nerwów obwodowych za pomocą specjalnych penów. Pozwalają one na określenie najbardziej odpowiedniego miejsca wprowadzenia igły, w dobie USG wydają się być mało użyteczne. Pomocne jednak bywają w trakcie nauki oraz treningów.
Igły do stymulacji
Obecnie wykorzystywane są wyłącznie igły całkowicie izolowane (izolowana jest nasadka oraz ostrze poza końcówką) w celu uniknięcia rozproszenia prądu stymulacji. Dostępne są także zestawy do ciągłych blokad nerwów obwodowych dające możliwość stymulacji nerwu przy użyciu izolowanego cewnika (tzw. stimulating cathrters, niedostępne w Polsce).
- Izolowana echogeniczna igła formy Pajunk
- Zestaw do blokad ciągłych z cewnikiem do stymulacji StimuLong Sono (Pajunk)
Technika wykonania blokady przy użyciu stymulatora nerwów:
- Wybrać ustawienia stymulatora: natężenie 1-2 mA, czas 0,1 ms, częstotliwość 2 Hz.
- Podłączyć igłę do bieguna ujemnego stymulatora.
- Biegun dodatni czyli anodę podłączyć do pacjenta z wykorzystaniem elektrody EKG (wcześniej dobrze odtłuścić skórę).
- Podłączyć strzykawkę z LMZ do wężyka igły i wypełnić igłę.
- O prawidłowym podłączeniu stymulatora i zamknięciu obwodu informuje nas najczęściej pojawienie się świecącej diody bądź charakterystycznego dźwięku (w zależności od typu aparatu).
- Wykorzystując technikę opartą o punkty anatomiczne wprowadzamy igłę do czasu pojawienia się odpowiedzi ruchowej.
- Zmniejszamy natężenie prądu do czasu zaniku stymulacji.
- Staramy się zlokalizować igłę tak aby najmniejszy prąd stymulacji wywołujący odpowiedź mieścił się w granicach 0,2 – 0,5 mA.
- Po prawidłowej lokalizacji struktury nerwowej wykonujemy próbę aspiracji oraz podajemy odpowiednią objętość środka miejscowo znieczulającego nie zmieniając pozycji igły.
- Unikamy podawania LMZ pod dużym ciśnieniem, przy prądzie stymulacji < 0,2 mA oraz w trakcie gdy pacjent zgłasza ból w trakcie iniekcji.
- Odpowiedź ruchowa najczęściej znika już po podaniu pierwszych kilku mililitrów środka miejscowo znieczulającego. Jest to zjawisko zwane jako „Raj test”. Początkowo myślano, iż jest spowodowane odepchnięciem nerwu przez podawaną substancję od końcówki igły. Zaobserwowano jednak, iż to zjawisko nie powstaje kiedy zamiast LMZ bądź roztworu chlorku sodu podawana jest woda. Mechanizm powstawania tego zjawiska jest dość prosty, otóż „sól fizjologiczna” jak i środki miejscowo znieczulające są roztworami elektrolitowymi, przez które przewodzone są ładunki elektryczne, co powoduje ich rozproszenie i co za tym idzie konieczność użycia większego natężenia prądu w celu uzyskania odpowiedzi ruchowej.
- Przy wykorzystaniu USG (dual guidance technique) stymulator nerwów bywa pomocny w celu potwierdzenia czy dana struktura widziana w obrazie ultrasonograficznym jest rzeczywiście strukturą nerwową, pozwala także ocenić odległość igła-nerw a także zmniejszyć ryzyko śródnerwowego podania LMZ (szczególnie gdy nie udaje się nam uwidocznić igły na całym jej przebiegu).
Podsumowanie:
- Odpowiedź ruchowa przy natężeniu > 0,5 mA – koniec igły najczęściej zbyt daleko od struktury nerwowej (wykonanie blokady najczęściej skutkuje niepowodzeniem).
- Odpowiedź ruchowa przy natężeniu 0,2 – 0,5 mA (0,1 ms) – optymalnie (wysoki odsetek skuteczności blokady).
- Odpowiedź ruchowa przy natężeniu < 0,2 mA – duże ryzyko śródnerwowej depozycji LMZ oraz uszkodzenia nerwu.
- Optymalny czas trwania impulsu – 0,1 ms. U pacjentów z zaburzeniami neurologicznymi pod postacią polineuropatii (np. pacjenci z cukrzycą) uzyskanie odpowiedzi ruchowej przy użyciu standardowej wartości czasu trwania impulsu (0,1 ms), może być niezmiernie trudne. W takim przypadku warto zwiększyć czas trwania impulsu do wartości 0,3 – 1 mA.
- Optymalna częstotliwość – 2 Hz.
Autor: W.Gola